 ����
����
�����ܵ��·�����ͯ��Ѫ�������ذ����Ŵ���������������Ⱦ������ȱ�����أ�����ÿһ����Ѫ��������˵������ȷ���������²�ԭ��
1.����
(1)�������أ��Ӵ�������������ڰ�Ѫ���ķ��������������սʱ�ձ�����ԭ�ӵ���ը���ذ�Ѫ������������֤ʵ��һ�㡣�Ӵ������Է���Ҳ���Ӱ�Ѫ���ķ����ʡ����ڽӴ������ж���ѧ��Ʒ�뼱�Է��ܰ�ϸ����Ѫ���йء�������ALL���������йصĻ�ѧ��Ʒ�г��ݼ���ɱ������и���ơ�����ҩ���̲ݼ���ѧ�ܼ�������Щ������ALL������ȷ�й�ϵ�в��϶���
(2)��Ⱦ���أ�Smith���о������и�����̥����Ⱦ������5�����¶�ͯ��ALL��Σ�ա���Ⱦ����ALLΣ�������ӵĻ��ƿ����Ǹ�Ⱦ���»�����IJ��ȶ������ӡ�����֤��EB������Ⱦ������L
3��ALL��أ�Ҳ��ALL������HIV��Ⱦ��صIJ������档
������������Ⱦ���ͯALL�߷������йء����ƹ�������״���ɽ���ĸ�����ڸ�Ⱦ����������Ⱦ���Խ���ALL��Σ���Խ����ɺ��ӵ����á�
ĸ��ι���ɽ���Ӥ����Ⱦ�Լ����ķ�����ι����ʽ���ͯ����Ѫ��(AL)������Ա�����һ��Ŀǰ�Ĺ۵�������ĸ��ι���ɽ��Ͷ�ͯ��Ѫ��������Σ�ա�
���Ⱦ��ص��������ذ������߽��֡�����Ӵ�ʷ��ҩ��Ӧ��ʷ(����ù��)�����ڱ仯�ȣ��������ͯ��Ѫ����ȷ������������ۡ�
(3)����ȱ�ݣ�����������ȱ�����ܰ�ϵͳ���������ķ��������ߡ�
(4)�����Ի���(�Ŵ�)���أ��������ױ�����ȷ��ʱ����2���º�14���ͬ��˫��̥ͨ����������ѧ�����о�֤�������Թ���ͬһ̥����ͬһϸ��������ͻ����ͬ��˫����ͬ��ALL�ķ�����һ�µġ��������ּ�����˫��̥û���ٴ��ĺ�����ѧ�ϵIJ��졣���˲²�ijЩ�����ӵİ�Ѫ��������Դ��̥�ڡ����ҽ�һ���Ʋ⸽�����ػ���������ص����ڳ�������κ�ʱ�䷢����Ѫ����Ϊ��֤��һ���裬�о�����������Ѫӡ�Ǽ�����еĿ�¡���뻼����ص������Ѫ������ںϻ�������(TEL-AML1)������t(12��21)��TEL�ķ���λ��λ�����ȱʧ֮����������BϵALL�������Щ�о���ʾ��ͯ�����ܰ�ϸ����Ѫ��Ϊ̥����Դ��
�б����Ѫ������(����ALL)ͬ���İ�Ѫ�������ʱ���ͨ��Ⱥ��2��4��������˫̥��һ��������Ѫ������һ��������Ѫ���Ļ���ߴ�25%����������ԽС����һ�������Ļ���Խ�ߣ����������䣾7��ʱ����һ�������Ļ������Լ��١�˵����Ѫ���ķ����������������Ŵ����ز��룬��ȷ�еĻ���������δʮ�����ˡ�
2.���� ������̬ѧ������ѧ���Ŵ�ѧ����(��MIC����)���ɷ�Ϊ�������͡����Ƽ�Ԥ�������������ء�
(1)��̬ѧ���ͣ�Ŀǰ����ͨ��
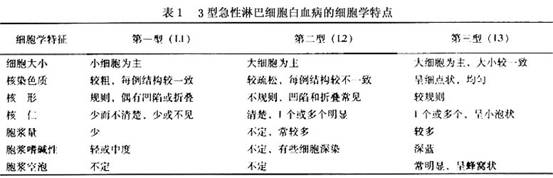
FAB���ͣ�������ϸ����С���˽����������ʴ�С����Ŀ�������ȼ�̶ȣ������ܷ�ΪL1��L3����(��1)��
С��ALL��L1��������ռ70%���ң�L2��Ϊ25%���ң�L3�ͽ�ռ0%��4%��
(2)����ѧ���ͣ���Ѫ������ѧ�ij������ѧ˵��Ϊ����Ѫ������Ѫϸ����ijһ��¡��������ijһ�ֻ����ϲ��쳣��ֳ�Ľ������˰�Ѫ��ϸ��������Ӧ������ϸ���ֻ��ε����߱�־���������á��ֻ��ء�(CD��cluster of differentiation)�Ե���¡����(McAb)ͳһ������
Ŀǰ��ALL��Ҫ��ΪTϸ��ϵ��Bϸ��ϵ�����ࡣ��ͯALL��Bϸ��ϵΪ����ռ80%���ҡ�Bϸ��ϵALL�ֿɷ�Ϊ�������࣬Ŀǰ����ͳһ�������Ҳ�һ���еķ�Ϊ4��(��2)���еķ�Ϊ6�͡�Tϸ��ѧALLһ���Ϊ3��(��3)��
���ڰ�Ѫ��ϸ�����С������ԡ��͡���ͬ���ԡ��������߱��͵ı������dz����������˿���ͬʱ���Ⱥ�������ֻ���������ϵ�е���������Ϊ�����Ѫ��(mixed lineage leukemia��MAL)���Ӻ���Ѫ��(hybrid leukemia��HAL)�������Ѫ��������Դ�ڶ��ܸ�ϸ����һ���Ϊ3�ͣ�
��˫���ͣ�ָͬһ����Ѫ��ϸ��ͬʱ������ϵ����ϵ������
��˫ϵ��(˫��¡��)��ָͬʱ���ھ�����ϵ����ϵ��������Ⱥ����ϸ��Ⱥ��
��ת���ͣ�ָ��Ѫ��ϸ����һ��ϵ������һ��ϵ��ת����
(3)ϸ���Ŵ�ѧ���ͣ�����ϸ���Ŵ�ѧ�ķ�չ���ر��Ǹ߷ֱ�ִ������Լ�����̽���Ӧ�ã�ʹ��Ѫ���ķ�������ǰ�ƽ�һ����Ŀǰ����90%���ϵ�ALL���п�¡��
Ⱦɫ���쳣��
Ⱦɫ���쳣���������쳣�ͽṹ�쳣��ALL��������Ϊ46��Ⱦɫ�壬�����Լٶ�����Ϊ�������Ϊ�������塣
�������쳣��
A.�������壺ԼռALL��1/4����ǰB-ALL�������Ȼ��������ۼ��κ�һ��Ⱦɫ�壬����4��6��10��14��17��18��20��21��XȾɫ�������
B.�ٶ����壺�����нṹ�쳣��46��Ⱦɫ�壬������ΪȾɫ����λ����L2�Ͷ����
C.�Ƕ����壺���ټ���Լռ3%��8%����45���߾Ӷ࣬һ��Ϊ20��Ⱦɫ��ȱʧ��
�ڽṹ�쳣����ͯALL�У��ѷ��ֽ�40�ַ������Ⱦɫ��ṹ�쳣������Լ50%ΪȾɫ����λ����������ȷ�����λ�����ڶ�ͯ��Ѫ�����ԣ��Ƚ���Ҫ�ͳ������У�
A.t(1��19)(q23��p13)������ڶ�ͯpre-BALL��λ��19p13��E2A������һ�ֿ��һ�������HOX������塣E2A/PBXI�ںϻ����pre-BALLԤ�������Ч���ϲ
B.t(12��21)(p13��q22)�����ǽ�Щ��ű����ֵ�һ�ֽ�Ϊ������Ⱦɫ����λ��λ��12p13��TEL�����������-��ת-�����ṹ��ͬ������һ��ת¼���ӡ�����������λ��ALLԤ��Ϻã�ԭ���塣
C.t(8��21)(q22��q22)��λ����Ҫ����AML-M2��λ��8q22��ETO������2��пָ�ṹ�����ܱ���һ��ת¼���ӡ���Ŀǰ��ΪAML1/ETO�ںϻ�����γɲ��ǰ�Ѫ�������Ĺؼ����أ������������Ŵ�ѧ�ı������ɷ�����
D.t(9��22)(q34��q11)������95%��CML��3%��5%�Ķ�ͯALL��������Ϊ����İ�Ѫ��Ⱦɫ����λ�������Dz�����BCR/ABL(break-point cluster region gene��abelson oncogene)�ںϻ����ⱻ��Ϊ��ϸ�����ĸ���ԭ�����⣬BCR/ABL�ںϻ�����Ϊ�Ǽ��С������(MRD)����Ҫ��־��
E.t(15��17)(q24��q21)������AML-M3���γ�PML/RAR���ںϻ�����������λ��AML-M3��ȫ��ʽάA�����ƽ����У�ͬʱ��PML/RAR��Ҳ����Ϊ�Ǽ��MRD����Ҫ��־��
F.inv(16)(p13��q22)������AML-M4Eo��Ⱦɫ�嵹λ�Ľ��������CBF��/MYHl1(ƽ����������������)�ںϻ���
G.�漰MLL�����
Ⱦɫ�������MLL����λ��11q23���ֳ�ΪALL1��HRX��Hrtx1������ת¼���Ӻ�DNA��ת��ø���������ԡ��漰����
Ⱦɫ���������t(1��11)��t(4��11)��t(6��11)��t(9��11)��t(10��11)��t(11��17)��t(x��11)�ȣ������Ӥ����Ѫ��������ALL��AML��MDS�ȣ���˱���Ϊmixed lineage leukemia gene������Ԥ���ϲ
���ڰ�Ѫ���漰��Ⱦɫ����λ����ڶ࣬��ο��ټ��ؼ����Щ������Ϊ�ٴ�ؽ����������⡣������ͯҽԺĿǰ�ѽ�������ʼ���ö���PCR�����������ϰ�Ѫ��������Ⱦɫ����λ��������ַ�������8��ƽ��PCR��Ӧ��ͬʱ���29�ְ�Ѫ����ص�Ⱦɫ��ṹ����/��λ(����87��mRNA���ӱ�����)��Ŀǰ�Ѽ���Ļ�����t(1��19)��t(7��10)��t(8��21)��t(9��22)��t(12��21)��t(15��17)��TAL1D��dup(11q23)��8��
Ⱦɫ�����(13�ּ��ӱ�����)��
(4)MIC���ͣ�1985��4���ڱ���ʱ�����MICЭ���飬����̬ѧ������ѧ��ϸ���Ŵ�ѧ����������ƶ���MIC����(��4��5)��
(5)�ٴ����ͣ��ٴ�һ�㽫ALL��Ϊ��Σ(standard risk��SR)��Σ(high risk��HR)�����ࡣ1998��6��ɽ���س��л�ҽѧ�����ѪҺѧ�顰С�����ܰ�ϸ�����ƽ��顱�������£�
����С��ALLԤ��ȷ����ص�Σ�����أ�
A.��12���µ�Ӥ����Ѫ����
B.���ʱ�ѷ���������ϵͳ��Ѫ��(CNSL)��(��)غ���Ѫ��(TL)�ߡ�
C.Ⱦɫ�����Ϊt(4��11)��t(9��22)�쳣��
D.С��45��Ⱦɫ��ĵͶ����塣
E.���ʱ����Ѫ��ϸ��������50��109/L��
F.�������յ�����60mg/(m2��d)��7�죬��8�죬����Ѫ��Ѫ��ϸ����1��109/L(1000/��l)����Ϊ�����ɲ���ЧӦ�ߡ�
G.��ΣALL�յ�����6�ܲ��ܻ���ȫ����(CR)�ߡ�
�ڸ�������Σ�����أ��ٴ����ͷ�Ϊ2�ͣ�
A.��ΣALL(HR-ALL)���߱������κ�һ������Σ�������ߡ�
B.��ΣALL(SR-ALL)�����߱������κ�һ��Σ�������ߣ����л���t(12��21)Ⱦɫ����ͺ͡�50��Ⱦɫ��ĸ߶�����BϵALL��
 ����
����
���ƣ���20�����������µĿ���Ѫ��ҩ�ﲻ�ϳ��֣��µĻ��Ʒ��������Ʒ������ϸĽ���ALL��Ԥ�����Ը��ơ��ִ��������Ѳ��ǵ�����û��⣬������ȡ���ڴ����մﵽ�����������������
1.ԭ�� ���ϻ����ǰ�Ѫ�����Ƶĺ��ģ����᳹���Ƶ�ʼ�ա���Ŀ���Ǿ���ɱ���Ѫ��ϸ����������ڵ���������Ѫ��ϸ������ֹ��ҩ���γɣ��ָ�������Ѫ���ܣ�����ﵽ��ȫ���⣬����������������֯�������������ڵĺ���֢��
ALL���Ƶ���Ҫԭ���ǰ��ٴ�Σ����ѡ��ͬǿ�ȵ����Ʒ�����ǿ��������������ǿ�һ��ƺͼ�ֳ��ڳ������ƣ�ͬʱ�������ڻ���Ԥ��CNSL�ķ��������ƹ�����Ӧ���й۲죬������Ч�Ķ�֢���ƺͲ���֢��Ԥ�������ƣ�������ϸ����˨���������ܽ��ۺ�����ˮ�������ƽ�⣬ƶѪ����Ѫ��DIC���������ر����ġ��Ρ����������ܵ�ά�֣����ָ�Ⱦ�����ֻ���ҩ�ﶾ�Է�Ӧ�ķ��Ρ�ͬ��������Ѫ��ϸ����ֲ�����������Լ������Բ���������CR�������ֲ��
2.ALL���� �����յ��������ơ���������ơ�CNSLԤ�������ơ����յ����ơ�ά�ֺͶ���ǿ�����ơ�
(1)��Ѫ���Ļ�����ǣ�
����ȫ����(CR)��
A.�ٴ���ƶѪ����Ѫ����Ⱦ����Ѫ��ϸ��������֡�
BѪ��Ѫ�쵰�ף�90g/L����ϸ����������ͣ�����������ϸ����ѪС�壾100��109/L��
C.������ԭʼϸ��������ϸ��(������ϸ��)��5%����ϸ��ϵͳ����ϸ��ϵͳ������
�ڲ��ֻ��⣺�ٴ���Ѫ������3������1��2��δ�ﵽ��ȫ���������������ԭʼϸ��������ϸ����20%��
��δ���⣺�ٴ���Ѫ�����������δ�ﵽ��ȫ���������������ԭʼϸ��������ϸ����20%�����а�����Ч�ߡ�
(2)�������ƣ��˽�����Ŀ�����ڰ�Ѫ��ϸ����û������ҩǰ���û��Ƶķ���Ѹ�������ȥɱ�˰�Ѫ��ϸ�����ָ�����������Ѫ����ͬʱ���ⷢ�������Ļ���ҩ�ﶾ�Է�Ӧ����Ⱦ��ͨ���ü���ҩ�����ϻ�����ɱ��99%�İ�Ѫ��ϸ��������ϸ����1012������108��ʹ������ԭ���ܣ�5%���ﵽCR��С��ALL���յ�����������Ӧ��2��ҩ��VPʹ90%����С����CR����L-ASP��CR�ʽ�������ߡ��ڸ�ΣС��ALL���������ġ�����ҩ���ϻ��ƣ�CR����Ȼ�����ӣ�����������ҩ�ﶾ�Դ����ķ��գ�����Ҫ���Ǽ��ٸ�������߳���EFS�ʡ��˽�֧�������DZ�֤ǿ����˳�����еĹؼ����������ע��ϸ����ѪС��ͷǸ�˾ͤ(G-CSF)��Ԥ�������Ƹ�Ⱦ��ʹ�����ܰ�ȫ�ȹ����������ڡ�
ALL�յ�����������ѡ�����ⳣ�õı�����VDLP�������������¼�(VCR)1.5mg/m
2��ÿ��1�Ρ�4�Σ�
���ù��(
DNR)30mg/m
2��ÿ��1�Σ���2��3��(HR-ALL��3�Σ�SR-ALL��2��)��
�Ŷ�����ø(L-Asparaginase��L-ASP)6000��10000U/m
2������1�Σ���6��8��(HR-ALL��8�Σ�SR-ALL��6��)��������(Prednisone)ÿ��60mg/m
2����3�οڷ�����28�죬��ͣ7�졣95%������28��35��ʱ�ܴ���ȫ����(CR)��
��Ѫ���ﻺ�����û�н�һ�������ƣ�ʣ��108��Ѫ��ϸ������ֳ�����¸�������CR���һ�����ٲ�����Ѫ��ϸ�������ư����������ơ�ά�����Ƽ�������ϵͳԤ�������ơ�
(3)��������ƣ��������ƻ����ǿ����ָ��CR���������м����Ƴ̵�ǿ�һ��ơ�����ǿ����������Щҩ�����Ϲ��̡�ǿ���ϸ�����������ͳһ�ķ�����
BFM��������ά�������������ظ��յ����ⷽ��VDLP������SJCRH����
���Ჴ����
���ǰ���(
Ara-C)�Ľ��˸�Σ��ALL��Ԥ��
�Ƽ���CAT��������������(CTX)800��1000/m
2��1�죬
���ǰ���(
Ara-C)ÿ��100mg/m
2��7�죬2��/d(ÿ12��Сʱ1��)��Ƥ��ע�䣬
��������(
6-TG)��������(6-MP)��ÿ��75mg/m
2������ٷ���7�죻HR-ALLʱ�ɲ����С������
���ǰ���(
Ara-C)��1��2g/m
2��ÿ12��Сʱ1�Ρ�(4��6)�Σ���������(CTX)��������(6-MP)ͬ�ϡ�
(4)CNSL�����������Ѫ��Ԥ�����������ڴ��ڡ�Ѫ-�Լ�Һ���ϡ��͡�Ѫغ���ϡ��Ȱ�Ѫ��ϸ������Ȼҩ���Աӻ����������Ѫ���ĸ���ֱ��Ӱ���Ѫ���Ĵ��ʱ�䣬����ȫ����������˱ӻ���Ԥ�����������������ӣ��������бӻ���Ԥ������40%��С��ALL��CR��3���ڷ���CNSL��CNSLռС��ALL������75%���к�7.7%����غ���Ѫ����CNSL��������Ϊ������ϵͳ�ǰ�Ѫ��ϸ���ıӻ�������������Ѫ��ϸ�������ALLʱ��DZ�룬����Ѫ�����ϵĴ��ڣ����õĻ���ҩ���糤���¼�(VCR)��
���ù��(
DNR)��
���ǰ���(
Ara-C)����������(CTX)��
�Ŷ�����ø(L-ASP)�Ȳ�����Ѫ������ɱ���Լ�Һ�еİ�Ѫ��ϸ��������������Ĥ����ֳ������CNSL���̶����¹��輰�������⸴������˱ӻ���Ԥ��������ʮ����Ҫ��Ӧ�ӻ���֮���Ϳ�ʼ���ᴩ����ά�����ơ���Ҫ��ʩ��
�ٲ��ô�����װ�����(HD-MTX)����ѪҺ���Լ�Һ�е�ҩ��Ũ�ȣ�����ЧԤ��CNSL��غ���Ѫ���ķ������յ����ƿ�ʼ��2��5����ÿ������ע��װ�����(MTX)��
���ǰ���(
Ara-C)����������(DX)������������1�Σ���5��6�Σ��Ժ�ÿ3����1�������ƽ������װ�����(MTX)����Ϊ12.5mg/m
2(���12.5mg)��
���ǰ���(
Ara-C)1mg/kg(���50mg)����������(DX)0��2��Ϊ2.5mg����2��5mg��
��ȫ������ҩ���в����Լ�ҺŨ�Ƚϸ�ҩ����
�����(VP
l6)��IDA��
�Ŷ�����ø(L-ASP)��Ȼ����ֱ��ͨ��Ѫ�����ϣ���Ҳ�ɼ����Լ�Һ���Ŷ�����ˮƽ����ɱ���Լ�Һ��Ѫ��ϸ�����á�
�����ڻ��ƣ�����ע��װ�����(MTX)��(��)
���ǰ���(
Ara-C)��Ԥ��������CNSL�п϶�����Ч,Ŀǰ�����Ű������������ע��ҩ��
������װ�����(HD-MTX)�ڹ����������ƽ�����ʼ��ÿ��10��15��1�Σ���3�Σ��Ժ�ÿ3����1�Σ���Σ(HR-ALL)����6��9�Σ���Σ(LR-ALL)����4��6�Ρ�ÿ�μװ�����(MTX)����Ϊ3000mg/m
2��1/6������ע15min(������500mg)��������24h�ھ��ȵ��롣����ע��30��120min����ע�롰���������ơ����������37Сʱ������
Ҷ����(CF)151mg/m
2��6��8�Σ�����ע���Ժ�ɸ�ÿ6Сʱ1�οڷ������������
Ѫ��MTXŨ��(��0.1mol/LΪ����Ũ��)���Ե�������
Ҷ����(CF)Ӧ�õĴ����ͼ�������44hʱ��1mol��68hʱ��0.1mol����CIF��6�μ��ɣ�����Ҫ�ӳ������ӽ�ȼ�����
Ԥ�����Դ�ʩ����ˮ���������ǰ3����ڷ�̼������0.5��1.0g��3��/d�����Ƶ�������5%̼������5ml/kg���Σ�ÿ�첹Һ1/5�ź�����Һ3000ml/m2��24h�ھ��ȵ��룬��4�졣��ҩǰ�Ρ������ܱ���������
���Է��ƣ����ƶ�С������������������Ӱ��Խ��Խ����������ǵĹ�ע�����Ŀǰ�����������ŷ����Է�����Ϊ������ϵͳԤ�����ƣ����������ƹ�����ÿ2����1����ע�������װ�����(HD-MTX)��ע��ͬʱ��ע��ֻ����CNSL������Σ���صĻ��������Է��ƣ����ҷ��Ƽ�����24Gy����18Gy��
(5)���յ����ƣ�һ���ڵ�3�δ�����װ�����(HD-MTX) ����
Ҷ����(CF)10��14����HR-ALL������ǿ�����Ʒ�2���Σ���1����VDLP�����յ����ƵIJ�֮ͬ����
���ù��(
DNR)�ͳ����¼�(VCR)ÿ��1�ι�2�Σ������ɼ���ÿ��45mg/m
2��14�죬������7����ͣҩ���ڷ�����2����
�����(
VP-16)ÿ��200mg/m
2��
���ǰ���(
Ara-C)ÿ��300mg/m
2��ÿ3��1�Σ���3�Σ����Ρ�SR-ALL������ǿ��ֻ��VDLP��
(6)ά�����ƺͶ���ǿ�����ƣ�������յ����⼰CNSLԤ�����ٻ��ƣ��������������ڣ���Ѫ���ͻḴ����ά������Ŀ���ǽ�һ�����ٰ�Ѫ��ϸ������Ҫ��ҩ������(6-MP)�ͼװ�����(MTX)����ϼ��ó����¼�(VCR)�������ɡ��������ƶ�60%��80%�ı�ΣALL����Ч���ܺܺõ����ܡ�������(6-MP)�ͼװ�����(MTX)��ǿ�ȶ������Ƿ��ܳɹ�����Ҫ�������е͵��ۼƼ�������һ���߸����ʡ���ά�������У���ϸ������������С��3.5��109/L��ALL�������ڰ�ϸ�����ߡ��ڷ�����ҩ����������ö��кܴ�ͬ��������ǵ���ʧ�ܵ�ԭ�ڷ�������������(6-MP)�ͼװ�����(MTX)��ѪҩŨ�ȿ���6��20��֮���˶�ÿ���������ѪҩŨ���ر���ϸ����ҩ��Ũ�ȼ��������������(6-MP)�ͼװ�����(MTX)�������б�Ҫ��������(6-MP)�ͼװ�����(MTX)�������ö�ͨ��ҩʱ������������Ϸ�ҩ�����Ϻá���ά��������ÿ��4��12�ܼӳ����¼�(VCR)��VP�����ۡ�������ͯҽԺ����ÿ��4�ܼ�����Щҩ��
����ǿ�����ƣ�����������������ά���������ڼ������յ�����ǿ�����ƣ���BFM����VDLP��������(6-MP)��
���ǰ���(
Ara-C)�ͻ�������(CTX)��CCG��VALD��SJCRH����
���Ჴ����
���ǰ���(
Ara-C)��
ά������ʱ�䣺ά��������Ҫ�ʱ���Ǹ�����������⡣������ALL���ٴ�CRһ����MRD���ԣ���2���������ಡ�˳������ԡ������Ͻ�����Ӧ����ֱ���������а�Ѫ��ϸ����Ϊ������ʱ�����ɶ�ÿ�����˶���ͬ��һ��������ʱ��2��3.5�ꡣ
�װ�����(MTX)��ע20��30mg/m2��ÿ��1�Σ���3�ܣ�ͬʱ������(6-MP)ÿ��75mg/m2����21�죬�ڷ�����ӳ����¼�(VCR)1.5mg/m2�Σ������ɼ���ÿ��45mg/m2����7�죻���ÿ4��1�����ڣ��ܶ���ʼ�������ݸ�������Ѫ��ϸ�����������װ�����(MTX)��������(6-MP)������ʹ��ϸ������ά����(2.8��3.0)��109/L��HR-ALL����ÿ12������VDLPһ�Ƴ�(ͬ���յ���һ��)��Ϊǿ�����ơ�SR-ALL�����������к�Ϊ3�꣬Ů��2.5�ꣻHR-ALL����ӳ�6��12���¡�
(7)CNSL���ƣ�����������������ע����8�Σ�����1�����Լ�Һ������ϸ����ʧ(һ����ע2��3�κ��Լ�Һ���ת��)���Ժ�ÿ��2�����ܹ�8�Ρ���CNSL�����ڹ���CR�ڣ��������Լ�Һת��������1��ȫ��ǿ�����ƣ��Ա���CNSL��ȫ��������Ȼ����ȫ����(60Co��ֱ������)���ƣ��ܼ���Ϊ18Gy���ֳ�15�����䣬�������㹻���ߵĴ����仼��ͬʱ��ȫ������ƣ���С���仼������ȫ���Ƶ�ͬʱ�������ڻ���ÿ��1�ι�2�Ρ�����ʱ����CNSL���������յ����ƽ�������ȫ��ȫ������ơ����ƺ�ÿ8����ע��������1�Σ�ֱ����ֹ���ơ�
(8)غ���Ѫ��(TL)���ƣ�غ���쳣�״���ΪTLʱ��������������ȷ���Ϊ˫��TL������˫��غ����ƣ��ܼ���Ϊ24��30Gy�����ǵ���TL����������غ�����(�Բ���Ϊ�������Բೣ��Ӱ��)��غ���г�������ʱ����TL��Ӧ��ԭ���Ʒ�������ȫ�����յ������̵����ƣ����յ���������TL�ֲ����ơ���CR�з���TL��������TL��ͬʱ������VDLDX��
�����(
VP-16)
���ǰ���(
Ara-C)������1���Ƴ���ȫ�����ƣ�������TL�������踴����
(9)����֢��Ԥ����֧�����ƣ�
�ٷ�ֹ����ϸ���ܽ��ۺ������ܰ�ϸ����Ѫ��ϸ���Ի��Ƴ�ʮ�����У��ڻ��ƿ�ʼʱ����������ϸ����ҩ��ɱ���ƻ��ܽ⣬��˶��շ�����ϸ���ܽ��ۺ�������������������ڻ��Ƹտ�ʼ1���ڣ���Ҫ����Ϊ������Ѫ֢����Ѫ�ء���Ѫ�ס���Ѫ�ơ���Ѫ�Ƶȵ�������ң����ƽ��ʧ������������DIC�ȡ�Ϊ��������ϸ���ܽ���ٶȣ���������ϸ���ܽ��ۺ����γɣ���������Ѫ��ϸ����������50��109/L�߳�ʼ����Ӧ��Լ����������������(ǿ����)�ͳ����¼��3��7���Ÿ����ǿ�Ļ��ơ��������յ��ڵ�1��2�ܵ��²��˾�Ӧ����3000ml/m2ˮ����5%̼������5ml/kg�ѪҺ����Һ��������ʡ����ᡢDICָ�꣬��֤ˮ�������ƽ�⣬ͬʱ���ñ��Ѵ�200��300mg(m2��d)���Լ���������γɣ���ֹ��������С��˨�����µ������ܲ�ȫ��
��Ԥ����Ⱦ��ע��ʳƷ���������������ٸ�Ⱦ���ᡣӦ��
�ǰ��ׇf��(
SMZ) 25��50mg/(kg��d)���յ��ڿ�ȫ��Ӧ�ã������ÿ����3�죬��ֹ���������ҳ���ס�����Ӧ����Ѫ������ÿ��200��400mg/kg���ܼ���ijЩ��Ⱦ�Ļ��ᡣ�����ڼ��ֹ���ֻ����磬�Ա�������ɢ����Ⱦ����ǿ��ǻ���Ż�������ʱ������ȣ�ݵ�DZ�ڸ�Ⱦ���Լ�����Դ�Ը�Ⱦ����ʱ����dz�������Ⱦ�Լ���������Ⱦ��
��Ӧ��
�Ŷ�����ø(L-ASP)��Ӧ��
�Ŷ�����ø(L-ASP)ʱ�˵�֬��ʳ�����ٺϲ����������Ļ��ע��Ѫ
����ˮƽ�����Ե���ʱ��ʱ���䣬�Ա���͵���Ѫ֢���ظ�Ⱦ�����ڽ����ġ��Ρ������ܼ�飬�����������ܲ�ȫ��
��Ӧ����Ѫ�̼����ӣ��ʵ�Ӧ����Ѫ�̼��������̹��������ڣ����ܼ��ٸ�Ⱦ���ᡣ��Ӧ��Ī��˾ͤ(GM-CSF)��Ǹ�˾ͤ(G-CSF)���Ի����в�����ǿ����48h����ݻ���ǿ����ʱӦ��3��5��g/(kg��d)����ϸ����3.0��109/L��
��Ѫ��ƷӦ�ã���ƶѪ����Ѫ��Ԥ����������ʮ����Ҫ��
(10)����벡�˹�����Ӧ����Ѫ��������Ϊһ��ϵͳ�Թ��̣���ü����˹���������ʮ����Ҫ�IJ��֣��Ա�֤��ʱʵʩ���Ƽƻ���Ҫ������ȷ��¼�ٴ�ʵ���Ҽ���������е����ƣ���ϸ���˽�����һ�ε����Ƽƻ�����Ժ���ע�����δ��ʱ��Ժ�������Ƽ����ʱ������ҳ���ϵ������ʧ���ߣ�����������ʺ�ͳ�Ƶ���ȷ�ԡ�
3.���������� С��ALL��������IJ�λ�ǹ��裬�����������ϵͳ��غ�衣�ټ�������λ���ܰͽᡢ��Ĥǻ���ǡ�Ƥ���ȡ�
����SJCRH���ϱ���80%С��ALL���ڴ�20%ALL�ڵ�1���ڷ����������ӵ�2�굽��4�긴��ÿ��Ϊ2%��3%��4����ٷ������¹�BFM�о���������������6��������������ڴ��������ǿ��ܵġ�
���������������ԭ�����Կ�¡��֯���������������ڸ�������Ҫԭ����Ϊ��ϸ����������ҩ��ż���и����İ�Ѫ��ϸ����MIC���Ͳ�ͬ�����ʱ�Ķ��Կ�¡������һ������ȫ��ͬ�ڰ�Ѫ���ļ̷�������������ͯҽԺ��1000����С��ALL����ֹͣ��4�����˷����ΰ������̷�������
�����������п��ܻ��2�λ��⣬��ȡ���ڵ�1�γ�����ȫ����ʱ�䡣��1��ʱ�����18������Ԥ�����2�λ�����ٳ������¡�ֻ��20%�����������CCRʱ�䳬��18���º���Щ�����ƺ�ͣҩ���������ò�ǿ�ҵ�ҩ���1�λ����Լ75%�ܻ��������λҲ�����Ƴɰܵ���Ҫ���������踴���ȵ������⸴����к��������ֵ�غ���Ѫ���������ٴ�غ�踴��������Ч��
(1)���踴�������踴�����˵����Ʊȳ��������ѣ��������ƹ����и���������ѡ��δ�ù���ҩ���Ӵ��������µ����Ʒ���������
�������(ȥ�������)��
���Ჴ����
�����������컷������
�������(
������ù��)�ȡ�ֹͣ���ƺ�ĸ����ɲ���ԭ�յ�������VDLD������Ӵ�ҩ�����������һ���⣬��������Ӧ��������ֲ(BMT)��BMT��CCR�ɴ�20%������������BMT�����������ǿά�ּ���ǿ���ƣ�CNSԤ������Ҳ�DZز����ٵġ�
(2)CNSL������������ALL�����в�ȡ��CNSLԤ�����ƣ�����5%��10%��������CNSL��CNSL�ɵ���������Ҳ�ɰ���踴�����������⸴����������������֢״������������CNSLԤ�������ơ�������ע��ʱ���������Լ�Һ���ʱ���֡�ĿǰCNSL��ϱ�Ϊ�Լ�Һ��ϸ��������5/mm3��ϸ�����ij�����������ϸ������CNS���۲����Լ�Һ���Է��֣�����CCG�о������Լ�Һ��ϸ��������5/mm3������TdT( )������ϸ�����Ҳ�ɳ�������Ȼ90%CNSL�����ܻ⡣��CNSL��������ͬʱ��̷����踴�����������⸴������˳��ڴ���20%��35%��Ӱ�컼���Ĵ�������У�����CNSL������CCRһ�����ϣ�CNSL����ǰ��������ע��δ�÷�����CNSLԤ��������Ԥ����Ϻá�
��CNSL��������������ע����1��3�Σ���2��2�Σ���3��4�ܸ�1�Σ�ͬʱ��ȫ����ǿ���ƣ�Ȼ����ͷ24Gy������12Gy���䣬�˺���ÿ8����ע1�Ρ������в���Ommaga����ȡ�ֲ���ڣ��������ڻ��ƣ�ҩ��ֱ��ע������ң�ʹҩ����ȷֲ�����������Ĥ��ǻ�����ɼ��ٷ��������̴�����ʹ�ࡣ���кϲ���Ⱦ��Σ�ա�
(3)غ���Ѫ����غ���Ѫ����������CCR 2���ֹͣ���ƺ��߽϶����
���о������ڻ��ƺ�2��3������ٴ�����������10%�к��������غ���Ѫ��������غ���Ѫ���緢���ڽ��ܻ����ڼ��20%��3��ij��ڴ������ƺ���48%���ڴ���ֹͣ���ƺ�����100%�ɻ��ڴ�غ���Ѫ�������Ծ�֢״��������Ӳ�ס���ʼ��Ϊһ���״������������ƿɲ����Բࡣغ���Ѫ����������Ҫ��ͬʱ������غ����з��ƣ�����24Gy��ͬʱ�����ȫ�����յ��������ơ�
���Ʒ����������������������ԭ����ͬ�����ϸ��ݸ������塢�����ص㼰�ٴ��������������Ŀǰ���ڳ��÷�����
�ٱ�Σ������
A.�յ��������ƣ�����VDLD����(28��)��
VCR(V)��1.5mg/(m2��d)(�����2mg/��)�����ƣ�ÿ��1�Σ���4��(d1��d8��d15��d22)��
Dex(De)��6mg/m2�ڷ�����3�Σ�1��21�졢��22�����ͣ1�ܡ�
DNR(D)��30mg/(m
2��d)����ע��1��2�졣
L-ASP(L)��5000U/(m
2��d)����ע�����죬��8�Ρ�����15�����ԭ�����ܣ�5%������L-ASP3�롣���Ƶ�15�츴����裬��δ���⣬ԭ������5%��20%��������L-ASP��ͬʱ��
DNRһ�Σ����28����δ��CR��ԭ�����ܡ�20%��Ϊʧ�ܲ�����Ӧ������������
���Ჴ�� ���ǰ���(
Ara-C)��Idarubincin
Ara-C�ȡ�
��L-ASP��������Ϣ6�죬���Ƶ�29�첢��������ϸ������ֵ(ANC)��1000ʱ�����¹��̷�����
B.��������(14��)������CAT������
��������(CTX)600mg/m2�����Σ��ڵ�1��ˮ�����Һ��
6MP 75mg/m2���ڷ���ÿ��˯ǰ1�Σ���1��7�졣��Ϣ7�������һ�Ƴ����ơ�
C.�ӻ���Ԥ��(30��)�����ô����������(HD-MTX) ����
Ҷ����(CF)��
��ANC��1000����������������ʼ��ҩ����3g/(m2��d)��ÿ��10��Ϊ1���Ƴ̹�3�Ƴ̡�����1/5��������(MTX)���ƣ�����4/5(������500mg/��)��6h�ھ��ȵ�ע���ھ��ư�����(MTX)��2h��ע1�Ρ��ھ��ư�����(MTX)��36h��CF��ȣ���һ��CF����Ϊ30mg/m2/�Σ����ƣ��Ժ�CF 15mg/(m2��d)���ڷ���ÿ6Сʱ1�Σ�42h��48h��54h��60h��66h��72h����7�Ρ��ô����������(HD-MTX)ͬʱ��VPһ��[VCR 1.5mg/(m2��d)��Pred 40mg/(m2��d)]�����켰������ˮ�����Һ����5%NaHCO3 80��100ml/m2��ע��ʹ��pH��7��ͬʱ���ֵ�Һ��2000��3000ml/(m2��d)��
D.����ǿ������(21��)��
���Ჴ�� 150mg/(m
2��d)����ע��ͬʱ��
���ǰ���(
Ara-C)300mg/(m
2��d)����ע����2��1�Σ���3�Ρ��Ƴ̽�����һ������Ϣ2�ܣ�Ѫ����ָܻ���
E.ά�����ƣ�VCR Dex��������(6-MP) ������(MTX)��������ƣ���1����VCR 1.5mg/(m2��d)����ע1�Σ�Dex 6mg/(m2��d)���ڷ���7�졣��2��4��������(6-MP)75mg/(m2��d)��ÿ��˯ǰ�ڷ�1�Ρ�3�ܣ�������(MTX)20mg/(m2��d)���ڷ��㣬ÿ��1�Ρ�3�ܡ�
F.����ǿ����
a.��1�μ�ǿʱ�䣺�Թ����CR���25�ܿ�ʼ������ΪVDLD 2�Ƴ̴����������(HD-MTX)��
�����¼�(VCR)��1.5mg/(m2��d)�����ƣ�ÿ��1�Ρ�2�ܡ�
�Ŷ�����ø(L-Asp)��6000ku/(m
2��d)����ע������1�Σ�����1�Ρ�6�Ρ�
Dex��6mg/(m2��d)���ڷ���14�졣
c.��3�μ�ǿʱ�䣺��2.5�꿪ʼ(����19������)������ΪCODDX 2�Ƴ̴����������(HD-MTX)��
G.����ע�䣺�յ����Ƶ�1��15��29���������ע���Ժ�ÿ8��������ע1�Σ���3����ÿ12����ע1�Ρ���ͬ������ע��������7��
�ڸ�Σ����:
A.�յ����ƣ�CVDLP 4�ܣ���������(CTX��C)800mg/m
2��ϡ����5%
������Һ100ml��1h�ڿ��پ�����ע����8��(1��)�������¼�(VCR)1.5mg/m
2(ÿ�������������2mg/m
2)����ע�䣬ÿ��1���ڵ�8�졢��15�졢��22�졢��29�죻
���ù��(
DNR��D)30mg/m
2����5%
������Һ100mlϡ�Ϳ��پ�����ע(30��40min)���ڵ�8��10�죬��3�Σ�
�Ŷ�����ø(L��ASP)5000��10000U/m
2������ע��ע(���ݲ�ͬ��Ʒ��������Ժ�����ѡ�ü�����ʩҩ;��)���ڵ�9�졢��11�졢��13�졢��15�졢��17�졢��19�졢��21�졢��23�죬��8�Σ�������60mg/(m
2��d)����1��28��(��1��7��Ϊ����������)��3��/d����29����ÿ2����룬1���ڼ�ͣ��
���ڸ߰�ϸ��Ѫ֢(��ϸ����100��10
9/L)�ߣ�������������
Ѫ���û�1��2�Σ�������������(��1��7��)��ϸ���ԣ�100��10
9/L�ߣ�
DNR�Ƴٵ���ϸ����50��10
9/Lʱ��ʼ����3�졣
���յ����⻯�Ƶĵ�19����븴�����ͿƬ�����ܳ���3�ֲ�ͬ�Ľ������M1�������������ƣ�ԭ�� ���ܣ�5%����M2������ʲ�ͬ�̶����ƣ�ԭ�� ����5%��25%����M3���������ƻ����ƣ�ԭ�� ���ܣ�25%��M1����ʾ��Ч��Ԥ�����ã�M2����ʾ��Ч�ϲ�����2��L-Asp��1��
DNR��M3����ʾ��Ч����������Ѫ�������뼰ʱ������Ϊǿ�ҵĻ��Ʒ�����
C.�����Ѫ��Ԥ�������ƣ�
a.������ע(IT)�����յ����Ƶĵ�1�������
���ǰ���(
Ara-C) Dex(����ͬ��)���˺��8�죬��15�죬��22��������(��������8)���յ��ڼ乲4�Σ�����ǿ�����ƽ�����1�Ρ�
b.HD-MTX CF(�����������-����
Ҷ����)�Ʒ����ڹ���������Ϣ1��2�ܺ���Ѫ��ָ��������������ϸ��(ANC)��1��10
9/L����ϸ����3��10
9/L���Ρ����������쳣ʱ���翪ʼ��ÿ10��1�Ƴ̣���3���Ƴ̡�
�����������(HD-MTX)3.0/m
2��1/5��(��������500mg/��)��Ϊͻ������30min�ڿ��پ������룬������6h�ھ��ȵ��롣ͻ����������(MTX)�����2h�ڣ�������IT 1�Ρ���ʼ��ע������(MTX)36h����CF��ȣ�����Ϊ30mg/m
2��������ע�䣬�Ժ�ÿ6Сʱ1�Σ��ڷ�����6��8�Ρ����������
Ѫ��������(MTX)Ũ��(��0.1��mol/LΪ����Ũ��)���Ե���CFӦ�õĴ����ͼ�����
�����������(HD-MTX)����ǰ����3��ڷ�̼������1.0g��3��/d���������Ƶ����5%̼������3��5ml/kg���Σ�ʹ��pH��7���ô����������(HD-MTX)���켰��3����ˮ������[2000��3000ml/(m2��d)]��
���ô����������(HD-MTX)ͬʱ��ÿ����������(6-MP) 50mg/m2����7�졣
c.�Է��ƣ�ԭ����������3�����ϻ����������ʱ��ϸ��������50��10
9/L��t(9��22)��t(4��11)�����ʱ��CNSL��������ԭ������HDMTX�����ߣ�����ȫ����(CR)��6����ʱ���У��ܼ���18Gy����15����3������ɣ�ͬʱÿ��IT 1�Ρ�������VDex��V
ADexÿ�ܽ��棬��2�Σ�VCR 1.5mg/m
2��ע1�Σ�Dex 8mg/(m
2��d)��7�죬�ڷ���
Ara-C 100mg/(m
2��d)��5�죬��2�Σ���ע��
D.����ǿ�����ƣ�����VDLDex��VCR��
DNR���ڵ�1�죬��8�죬����ͬǰ��L-Asp 5000��10000U/m
2����2�졢��4�졢��6�졢��8�죬��4�Σ�Dex 8mg/(m
2��d)����1��14�졣��3�ܼ�ͣ����Ϣ1��2��(��Ѫ��ָ��������������쳣)����
���Ჴ��(VM
26)
���ǰ���(
Ara-C)3��(�������÷�ͬǰ)��
E.ά�ּ���ǿ���ƣ�
a.ά�����ƣ�VDex/������(6-MP) ������(MTX)������������(6-MP) 75mg/(m2��d)��ҹ��˯ǰ�ٷ���21�죻������(MTX) 20��30mg/(m2��d)����ע��ÿ��1�Σ�����3�ܡ�����VDex����˷��������ҩ����ǿ������ʱ��ͣ��
��������(6-MP) ������(MTX)��ҩ3��ĩ���ְ�ϸ������3��109/L���ң�ANC 1.0��109/L�����ݰ�ϸ����ANC����������������(6-MP)�Ͱ�����(MTX)������
b.С��ǿ���ƣ�CV
ADex����ά��������ÿ���3����9���¸���1�Ƴ�(CTXΪ600mg������������÷�ͬǰ)��
d.δ���Է����ߣ�ά�����Ƶ�2���½��д����������(HD-MTX) ����
Ҷ����(CF)���ƣ�ÿ3����1�λ�ÿ6����2�Σ���8�Ρ�Ȼ��ÿ3����������ע1�Ρ����Է����ߣ��������������������(HD-MTX) ����
Ҷ����(CF)���ƣ�ֻ�ܲ���������עÿ12��1�Σ�ֱ����ֹ���ơ�
F.���Ƴ̣���ά����������Ů��3�꣬�к�3.5�ꡣ
4.������ֲ ������ֲ(bone marrow transplantation��BMT)���ư�Ѫ����ͨ��ֲ����ܸ�ϸ����ʹ��Ѫ��������ǿ�һ��ƺͷ��ƶ��ܵ������Ĺ��蹦�ܵõ��ָ�����ͨ����ֲ�������ֲ���Ѫ������(graft versus leukemia��GVL)�����ƺͷ��ƺ���������Ѫ��ϸ��(minimal residual leukemic cell��MRLC)������������BMT�����ͷ������ϸĽ�����ֲ�ɹ�������֮��ߣ�Ϊ��Ѫ�������ƿ�����һ���µ�;�����������ϻ��ƶ�ALLЧ���Ϻã����Ȳ�����BMT���ơ������ڲ��ָ�Σ�����������εIJ�����BMT����������Ч�������ֶΡ��μ�������ֲ��
 Ԥ��
Ԥ��
Ԥ����Ȼ���̽϶̣��������ƣ�һ�����6������������ƽ������Լ3���¡��Դ�Ӧ�����ϻ���������Ԥ���������Ը��ơ������ʿɴ�95%���ϣ�Ŀǰ���������¹�BFMЭ���飬����St.Jude��ͯ�о�ҽԺ(SJCRH)��5�����������Ѵﵽ80%������5���������ʴ�74%���ϡ����ų����������ʵ���ߣ�������ALL������Զ����������Խ��Խ�ܵ����ӡ�ͨ���������������ġ��Ρ��Ρ��������������Լ��˶����ܡ��������ȷ������õ��飬��Ϊδ���ܷ��Ƶ�ALL�������ɽ��������档Ŀǰ��ͯALL����Ϊ��һ�ֿ������Ķ���������
1.����ǰ��Ԥ������ С��ALL��Ԥ�����ڳ���ALL��Ӱ��С��ALLԤ�����غܶ࣬������Ÿ��ݲ�ͬ��Ԥ�����ؽ�С��ALL��Ϊ��Σ��Σ������(��9)����Щ���ŷ�Ϊ��Σ����Σ����Σ�͡�����С��ALLԤ��Ӱ��ϴ��������Ҫ���������䡢��ϸ��������Ⱦɫ��ı䡢����ѧ����̬ѧ���ͣ��Լ��Ƿ�ϲ�CNSL�ȡ�Ŀǰ���ϵ�Ӱ��Ԥ������Ҫ���أ�
(1)���䣺�������������϶���������Ҫ�Ķ������ء�2��10���С��ALLԤ��ã�CR�ʿɴ�95%��5�����¼�������(EFS)��70%���ϡ�������С��12���µ�Ӥ��Ԥ��������Ӥ�����Ⱦɫ��t(4��11)��λ�ͼ����Ӻ���Ѫ���йء�
(2)����Ѫ��ϸ�������������о���������ϸ��������CR�ʼ�EFS����ʮ����Ҫ��Ӱ�졣��ϸ��������Ӱ��С��ALLԤ����ؼ����ء�һ����Ϊ��ϸ����50��109/L��Ϊ��Σ���ء����۶�ALL��AML���߰�ϸ������100��109/L���ٴ�������CR�ʵͣ�����ڶ̣�Ԥ��
(3)ϸ���Ŵ�ѧ�쳣������Ⱦɫ��ִ������ķ�չ���������е��о����϶�
Ⱦɫ���쳣��ALL��CR������ھ���ʮ����Ҫ�����塣���ж���Σ���صĹؼ�ָ�ꡣPH
1( )ALL
Ⱦɫ���쳣�ж�ͯռ5%�����Ǵ���ڶ̣�Ԥ����鲡�˵�BCR-ABL�ںϻ���t(9��22)Ⱦɫ����λ�����֡���
Ⱦɫ���쳣��t(9��22)��t(4��11)Ԥ�������t(4��11)ALL����ǰB-ALL�����߱��Ͳ���ͬʱ������ϵ��ԭ����ʾ����ALL����Ϊ�����ڵĸ�ϸ����Դ��
(4)����ѧ���ͣ�����ǿ���Ƹı�ALL���ͺ�Ԥ���Լ�ϸ��Ⱦɫ�弼���о������룬����ѧ������Ԥ��Ĺ�ϵ�ı��治����ͬ����ȥ��ΪCD10 ALLԤ��Ϻã��µ��о�����CD10 ALL��Ԥ��û���Ҫȡ���Ƿ����Ph1( )��BCR-ABL�ںϻ���һ����Ϊ�ڶ�ͯALL������ǰB-ALL��C-ALL��ǰB-ALL����Ԥ��á�B-ALL�ټ���ռ1%��2%�����������L3����̬ѧ�����Ͳ�����(Burkitt)�ܰ�����ϸ���Ŵ�ѧ��������ȥ��ΪԤ������ǿ����Ӧ�ó���Ϸ���Եĸı䣬��ͯB-ALL���ڴ��ɴ�50%���ϡ�T-ALLԼռALL��10%��15%�������10�������곤�������߰�ϸ�����ݸ�����Ԥ��ϲ��ALL����ϵ��ԭ����(My )��Ԥ�������в�ͬ�۵㡣һ����Ϊ��ͯALL����ϵ��ԭ����(My )Ԥ�����岻����ΪALL��CD34�����Ԥ�������һ���о�֤ʵ��
(5)��������Ѫ������λ������Ϊ�иΡ�Ƣ���ܰͽ��״�Ԥ������Щ���س���ϸ���Ŵ�ѧ�쳣������ѧ���͡����䡢��ϸ�������ص�Ӱ�졣һ����Ϊ����ʱ�ϲ�������ϵͳ��غ�����ۼ��ݸ�������Ԥ������ָ�ꡣ
�����������ֱ������֡�3����Ϊ��ΣALL�����ֲ���3����Ϊ��ΣALL��
�������������У��������������Ѫ��ϸ������������Ҫ��Ԥ�����أ����о�ָ����������ռԤ�����ر��ص�60%�����ϸ��������100��109/L,���ϲ�������ϵͳ��Ѫ�������ϸ��������50��109/L������С��1������10�꣬��4���������ʽ�Ϊ64%��
2.������ص�Ԥ������ ��������ͨ��������ĵ�ALL��Ч�ܽᣬ�������Ʒ�Ӧ��Ԥ�������ܴ���������ÿ��60mg/m2 1�ܣ�����Ѫ����ϸ����1��109/L��Ϊ��Σ���أ��˼�Ϊ�������յ�����(prednisone induced test)��ͬʱ�����֣����������[��������ϵͳ��Ѫ����(��)غ���Ѫ��]��ALL��Ϊ��Σ���ء���Ҫȷ��������ϵͳ��Ѫ������Ҫ���Լ�Һ���ҵ���Ѫ��ϸ����
��һ�����Ʒ�Ӧ���յ��������ƺ��19�츴����裬���ܳ���3��������ٹ����������ƣ�ԭ�� ���ܣ�5%���ڹ���ʲ�ͬ�̶����ƣ�ԭ�� ����Ϊ5%��25%���۹������ƻ����ƣ�ԭ�� ���ܣ�25%�����е�1�����Ԥ��Ϻã���3�����Ԥ��ϲ����ʱ��ΧѪ��������ϸ��������������е�ԭ�������ܶ��٣���ΪԤ������ָ����
(1)����Ҫ��������ص��������յ��������ƴ�CRʱ�䡣�о����������ƺ�5���ڣ�����Ѫ������ϸ������һ����ƺ�2�ܹ�����ԭ���ܰ�ϸ���½���5%���µ�Ԥ��á�������ͯҽԺС��ALL�յ����������У�����ǿ���ƺ�90%���ϵĻ�����2��ʱ�����CR���������������ڣ�ʹ��Σ����Σ�͵�5��EFS����74%��
(2)�����CR��С������(minimal residual disease��MRD)������Ҳ����Ҫ����С��ALL�������ֳ��ڵ�ά�����Ƽ��ӻ�����Ԥ�����ƣ��Ƴ���2.5��3�ꡣ
(3)ԭ���ͼ̷���Ѫ����ҩ�ǻ���ʧ�ܵ���Ҫԭ��ʮ�����Զ�ҩ��ҩ(MDR1)���ٴ��о���չѸ�٣�����ʹMDR1������ת���Ӷ��˷��������еIJ������ء�
Ӱ��С��ALL��Ԥ�����غܶ࣬��������������Ӱ��ġ����������Ǻܸ��ӵĻ��壬�����ػ�����ػع�����ȷ����о����о����ԡ�����ǰΣ�����������䡢��ϸ������ϸ���Ŵ�ѧ�쳣�ȶ�Ԥ��Ӱ��ϴ�ͨ���������Ʒ�����ǿ�һ��ƣ����廯���ƻ���ù�����ֲ�����Լ���ALL��Σ�����ء�
3.�ж�Ԥ���ָ�� Ϊ���ݶ�������Ӱ��ALL����ʶ��1998���л�ҽѧ����Ʒֻ�ѪҺѧ����ɽ���ٳɶ������ж�Ԥ���ָ��Ϊ��
(1)С��1���Ӥ����Ѫ����
(2)���ʱ����������ϵͳ��Ѫ����غ���Ѫ��(��������ȷ�������Ѫ�����ٴ�����)��
(3)Ⱦɫ�����Ϊt(4��11)��t(9��22)�쳣��
(4)����45��Ⱦɫ��ĵͶ����塣
(5)���ʱ����Ѫ��ϸ����50��109/L(��ʷ������Ѫ��ϸ���й���50��109/L)��
(6)�������յ������8�죬����Ѫ����ϸ����1��109/L��
(7)��Σ����(SR-ALL)�յ�����6�ܲ��ܻ����ȫ�����ߡ�
�߱������κ�һ�������߾�Ϊ��Σ���ܵ�������ݡ����߱������κ�һ���Ⱦɫ����t(12��21)�ı��B-ALLΪ��Σ���ܡ�



 ���в�ѧ
���в�ѧ
 ����
����




 ��������
��������
 �ٴ�����
�ٴ�����
 ����֢
����֢
 ʵ���Ҽ��
ʵ���Ҽ��

 �����������
�����������
 ���
���
 �������
�������
 ����
����
 Ԥ��
Ԥ��

 Ԥ��
Ԥ��